PEXIVASの結果が出版されて早10ヶ月。当初は結果だけを聞いて「脱力」したことを覚えています。
これまでリウマトロジストは喀血するAAV患者にせっせと血漿交換をしていたのでした。患者を助けることが出来た、というやりがいを感じながら....
その際、肺胞出血または透析中のAAV患者は血漿交換でANCAを急速に下げることで予後を改善できることを信じていたものの、重症腎不全にはMEPEXというRCTの結果があるが、肺胞出血に関しては観察研究だけでエビデンスが危ういこともなんとなく感じていました。
この度、よくデザインされた肺胞出血 or 腎不全を対象とし血漿交換とステロイドの減量レジメンを同時に検証したRCT、PEXIVASを勉強してみました。
Plasma Exchange and Glucocorticoids in Severe ANCA-Associated Vasculitis
Walsh M, Merkel PA,,, Jayne DRW (PEXIVAS Investigators)
https://www.nejm.org/doi/full/10.1056/NEJMoa1803537
Methods
Trial Design
この重症で活動性AAV患者のRCTは2×2因子のデザインであり、PEで初期治療を行う事をPEなしと比較し、また2つのステロイドレジメンを比較することができた(全例にCY or RTXを投与したうえで)。試験の目的、デザイン、方法は過去に報告され、2014年に変更された最終的なプロトコールはNEJM.orgで入手できる
https://www.nejm.org/doi/10.1056/NEJMoa1803537
Trial Oversight
Cambridge大学のNHS財団が試験を注意深く観察した。(略)治験管理委員会(the first, second and last authors)が調査者からの協力を元に試験をデザインし、統計の計画を用意し、データの正確さと完遂性、プロトコールの厳守性を保証した。
Patients
June 2010 - September 2016の間に登録した。詳細はSupple appのSection S2。簡単に言うと15歳以上で、新規or再発性のGPA or MPA、MPO or PR3-ANCA+の既往、腎障害、または肺胞出血を伴う肺病変。
Inclusion criteriaの詳細はappendixより以下でした。
https://www.nejm.org/doi/suppl/10.1056/NEJMoa1803537/suppl_file/nejmoa1803537_appendix.pdf
1.新規or再発のGPA、MPA(CHCCに基づく)AND
2.ELISAでPR3- or MPO-ANCA (+) AND
3.重症の血管炎;以下のいずれか
a. i. 腎生検で局所的な壊死性糸球体腎炎 or 糸球体性血尿/円柱を伴う尿蛋白 AND
ii. eGFR<50 ml/m/1.73m2 (3ヶ月より長くeGFR<50なら除外)
b. i. 活動性血管炎による肺胞出血 AND
ii. その他の原因(うっ血や感染等)の除外 AND
iii. 1). BALで肺胞出血の確認 or
2) 喀血の観察 or
3) 原因不明の貧血<10g/dL or Hb<10ならHb drop >1g/dL
4) DLCOの増加
4.患者or保護者の同意
Treatments
患者はインターネットを用いた中央割り付けシステムで1:1:1:1でPE+標準GC、PE+減量GC、No PE+標準GC、No PE+減量GCに分けられた。全例がCY or RTXの投与を受けた。Randomizationは最小限のアルゴリズムの使用を用いて行われた。すなわち 層別化は以下に基づいた;60歳未満か以上、腎障害(Cr<5.6mg/dlか以上か)、ANCAサブタイプ(PR3 vs MPO)、肺胞出血の重症度(無しか、非重症 vs 重症の出血;重症はSpO2 85%以下か人工呼吸器管理で定義)、導入療法(CY or RTX)。全ての患者と調査者が治療グループの割り付けに気づいていた。
Randomizationの前にCY (静注or経口)かRTXの選択は各地の医師によって決められた。ステロイドのレジメンについては全例が地方の医師の判断で注射のmPSL1-3日で治療された(最大累積投与量1-3g)。全例が体重(<50、50-75、>75 kg)に基づいてPSN or PSLを投与された。標準レジメンは同時期の国際trialで用いられたレジメンの修正に基づいて行われ、調査者のmeetingでの総意によって決められた。減量レジメンと標準レジメンのグループは最初の週に同じ治療を受け、第2週の開始時から第1週と同じ投与量または約50%減量で投与された。標準治療はweek3より減量が緩徐に行われた。減量レジメンの6ヶ月後の積算量の違いは標準量のそれの<60%。22wks以降は両群とも5mg/dayをwk52まで続け、この時に各地の医師がその後の経口GCの量を決めた。
Table S3. Dosing for oral Glucocorticoids in the standard and reduced-dose limbs from trial start.

PEを受ける患者はcentrifugation or filter separationの方法でアルブミン60 ml/kgの補充を受けた;randomization後14日以内に7回の治療を受けた。出血リスクが高い患者では血漿交換が許可された。
難治性or早期の再発性疾患がrandomization後に起きた患者は追加のステロイドパルス療法でPEなしで治療された。CYの3-6ヶ月後、患者はAZPの維持療法を少なくとも52wkまで投与された。その後の維持療法は各地の医師の判断で選択された。Randomizationから2017/7/30に最もコモンな完了の時期までフォローされた。プロトコールは最低2年のフォローを条件として課していたが、これはrandomizationから12ヶ月未満でほとんどのイベントが起きることを示す集計データの調査が出てからはもっともコモンな完了の時点まででよいこととされた
Outcomes
Primary outcomeは死亡or ESKD。ESKDは12wk以上の持続的な腎代替療法(血液透析or腹膜透析)or腎移植と定義された。secondary outcomeは死亡、ESKD、持続的寛解、重症AEs、1年以内の重症感染症、健康関連QOL(これらの定義はSection S7に記載)。持続的寛解を評価するためGPAのためのBVAS score(BVAS/GPA)を疾患活動性の評価に用いた。QOLはSF-36, ver 2とEQ-5D index score、health thermometer scoreを用いて評価した。
Statistical Analysis
PE vs Non PEの比較のために164例のPrimary outcome eventsの発生があれば80%のパワーでHR 0.64を検出するであろうと計算した(two-sided alpha level of 0.05で)。過去のtrialsのデータを元に500例が登録され2-7年のフォローが必要であろうと見込んだ。2014年、その時までに登録された患者における死亡orESKDの率のレビューを行ったところ164のイベントを得るために675-725例の大きなサンプル数が必要であろうことが示唆された。そのため700例を最低1年のフォロー期間で登録することを計画した。これらの計算はPEとnonPEとの差がないことを想定して行った。
2つのステロイドレジメンはnoninferiorityの仮説で比較された。noninferiority marginはPEとNonPEとの比較のために計算されたサンプルサイズに基づいて計算された。700のサンプルサイズでもって減量レジメンにおけるESKDor死亡の発生率が標準量に比べ11%高い事を示すパワーが80%よりも高いであろうことを想定した。one-sided alpha level of 0.05において。
統計解析はSAS software, version 9.3 and higher (SAS Institute)を用いた。(略)全ての解析においてreference armはno PEと標準GC。lost to follow upまたは脱落した患者や打ち切りの患者or primary outcomeのデータはprimary outcomeの状態が分かる最後の日で打ち切りとした。統計解析は多様性の補正のための対策を含まなかったため、secondary and other outcomesはポイントの推定と95%CIで報告された。CIの広さは多様性のために調整されていないため間隔はsecondary outcomeの確かな治療効果を推定するために使用されるべきでない。
PEの解析のために全患者が割り付けされたグループに応じてITT解析で評価された(★PEはITT解析★)。死亡 or ESKDのprimaryの複合アウトカムがCox proportional-hazards modelを用いてHRと95%CIを求めるために使用された。
GCレジメンの評価において私たちのprimary objectiveは減量GCレジメンがprimary composite outcomeに関して標準レジメンに比べ劣っていないことを決定することであった。ITT解析は誤ってnoninferiorityを示すリスクを増やす可能性があるため、primary analysisのためにper protocol人口を用いた(★GCレジメンはPP解析★)。私たちはper-protocolの人口を標準レジメン群は最初の6ヶ月でプロトコールで定められた投与量の少なくとも70%を内服した患者、減量GCでは最初の6ヶ月で定められた投与量の130%を超えない量を内服した患者と決めた。Primary composite outcomeのリスクにおいて両群間の絶対的なリスクの差とその95%CIをnon-inferiority margin 11%の絶対リスク差を比較するためのbinomial model with an identity-link function を用いて計算した。Primary outcome は標準GCと減量のレジメンにおいて、per protocolとITT人口のためのHRと95%CIを得るためのCox proportional-hazards modelを用いて評価された。(→hazard比はPPとITT人口の両方で検討)。その他すべてのoutcomeの解析はITT解析で行われた
Secondary outcomesのため、任意の原因による死亡とESKDはCox proportional-hazards modelを用いて別々に解析された。持続寛解を達成した患者の数と少なくともひとつのsAEを経験した患者の数は群間で比較された。相対リスクを得るためのlog-binomial regression modelを用いて。1年目および試験終了時までの重症感染症の率はnegative binomial regressionを用いて解析された。発生率の比を得るために患者が試験に滞在した期間の長さを補正して。健康関連QOLアウトカム@1年の差は治療群の時間の相関を必要に応じ含んだlinear mixed-effects models for repeated measuresを用いて推定された。
私たちはPrimary outcomeに関するあらかじめ決められたサブグループ解析を最小限のグループで行った。以下の3つのあらかじめ定められたsensitivity analysesを行った:①解析を1年のフォロー時に絞って行った;②PEの効果をper protocol populationを用いて行った。これにはrandomizationから14日以内に死亡した患者、PEに割り付けられ少なくとも1回のPE治療を行った患者、14日以内にcontrolに割り付けられたPEを行わなかった患者を含めている。③さらにITT解析で2つのGCレジメンの人口を評価した。またpost-hocのsensitivity analysisを行い、ITT人口において2つのGCの群間の絶対リスク差を計算した。
Results
Figure S1. Plasma exchange participants

Figure S2. Glucocorticoid dosing participants

Table 1. Characteristics of the Patients at Baseline.*

Patients
フォローの中央値は2.9年。16ヶ国の95センターで704例が登録され、352例がPE、352例がNo PE、353例が減量GC、351例が標準GCに割り付けられた(Figs. S1 and S2)。フォローの中央値は2.9年。ベースラインはTable 1のとおり。PE群の338例(96.0%)、control群の322例(93.5%)がper-protocol populationに含まれた。減量330例(93.5%)、標準325例(92.6%)がper protocol populationに含まれた。
Outcomes
According to Plasma Exchange
primary outcomeに関してGCレジメンとPE割り付けとの間に相関はなかった(p=0.72)。PEのprimary outcomeに対する効果をTable 2とFigure 1Aに示す。Death or ESKD はPE群で100/352 (28.4%)、No PE群で109/352 (31.0%) (PEのハザード比, 0.86; 95%CI, 0.65 to 1.13; P = 0.27)。1年で中止されたデータを含む解析を含んだsensitivity analysesの結果はprimary analysesのそれとあまり変わらなかった (Table 2)。サブグループ間での相関は見られなかった (primary outcomeのサブグループ解析はFig. S3.)

Figure 1A. Primary Outcome According to Plasma Exchange
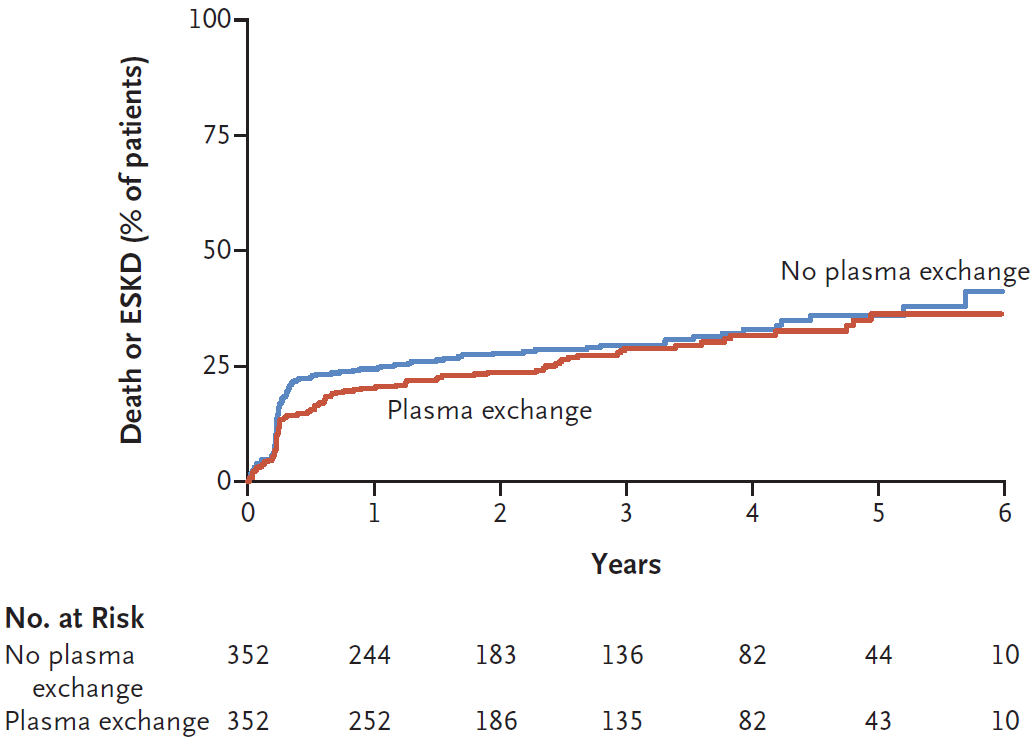
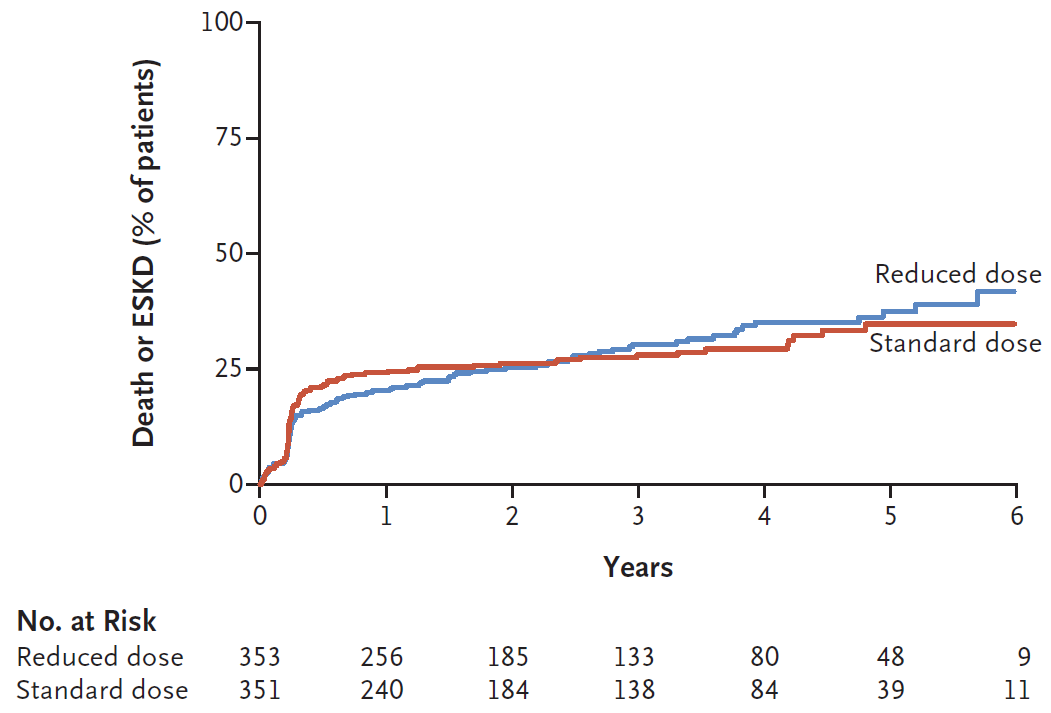
Figure 1B. Primary Outcome According to Glucocorticoid regimen
Secondary outcomesはTable 3 and Table S4にサマライズされている。PEとNo PEで重症AEsを含むsecondary outcomesに差はなかった。

Outcomes According to Glucocorticoid Regimens
減量のPrimary outcomeに関する効果はFigure 1B。Per protocol人口でdeath or ESKDは減量レジメンで92/330 patients (27.9%)、標準レジメンで83/325 (25.5%)。減量は標準に対しprimary outcomeに関して劣ってはいなかった(absolute risk difference, 2.3 percentage points; 90% CI, −3.4 to 8.0; 95% CI, −4.5 to 9.1)。ITT解析のsensitivity analysisでも同じく:107/353 (30.3%) vs 102/351 (29.1%) (absolute risk difference, taking into account differential follow-up time, 0.01 percentage points; 95% CI, −5.1 to 5.1)。生存曲線を用いてprimary outcomeの解析をするとPP人口でHR 1.04 (95% CI, 0.81 to 1.33)、フォロー中のデータを用いたITT人口で1.00 (95% CI, 0.76 to 1.31)、1年で打ち切った場合0.80 (95% CI, 0.58 to 1.10)。サブグループによる相関はなかった (Fig. S4)。
Randomizationから1年の間で142例の重症感染症が減量群で96例(27.2%)、標準量で180件/116例(33%)に起きた(incidence rate ratio, 0.69; 95% CI, 0.52 to 0.93)。その他のsecondary outcomeはいずれも両群間で有意差はなかった (Table 3).
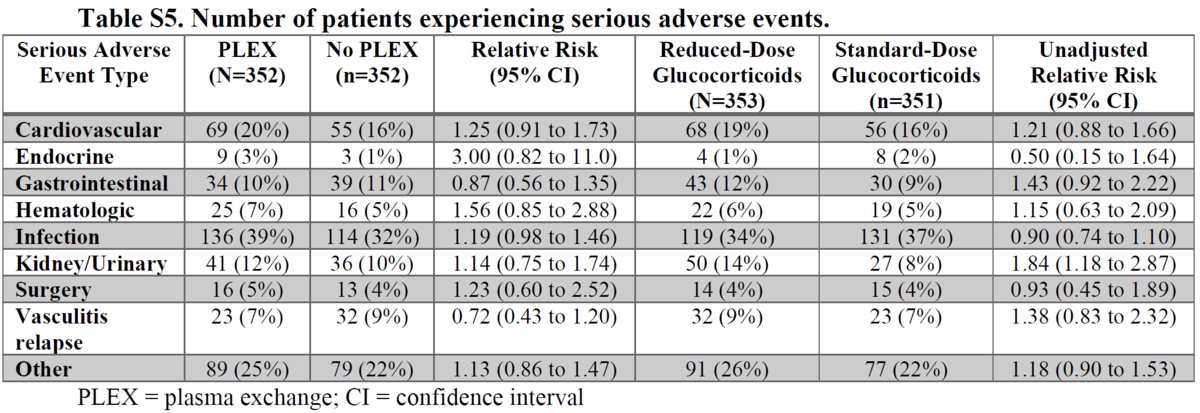
重症AEのタイプと頻度は減量vs標準で同様(コモンなものをTable S5に示す)。腎関連の重症AEは減量で多かった (unadjusted risk ratio, 1.84; 95% CI, 1.18 to 2.87)。ESKDでは同じであったが(hazard ratio, 0.96; 95% CI, 0.68 to 1.34)。
Table S5
<リウマトロジストのコメント>
・まず同じ集団をこのように2×2因子で分けて、かといって4群比較ではなく、2つの疑問を解決するという一石二鳥的なRCTははじめて読みました。その巧妙な方法に感銘を受けました。これからは、こういうRCTが増えてくるのでしょうか。
・血漿交換は1年後の負のアウトカム(死亡or ESKD)を減らすことに失敗し、フォロー期間中についても同様でした。もう血漿交換をする理由がないですね。これまでの自分のやり方を変えないといけないのかもしれません。
・標準ステロイド群は減量群に比べ重症感染症を増やすという結果でした。以上から新しい減量レジメンが望ましいのかもしれません。
(20210913追記)
・RTX or CYで結果がどうであったのかを見たくなってSubgroup解析をチェックしました。↓のFigure S3においてIVCYとRTXではややPlexに引っ張られているように見えました。いずれも有意差つかず。またFigure S4でRTXでは標準ステロイド量に引っ張られているように見えました。なので、必ずしも減量レジメンが良いとは言えないように思いました。
https://www.nejm.org/doi/suppl/10.1056/NEJMoa1803537/suppl_file/nejmoa1803537_appendix.pdf
Figure S3. Results of subgroup analyses of the effect of plasma exchange on the primary
outcome of death from any cause or ESKD.

Figure S4. Results of subgroup analyses of the effect of a reduced-dose regimen of oral
glucocorticoids on the primary outcome of death from any cause or ESKD.

(2021/10/1)
肺胞出血でPLEXをすべきか否かを決めるため、Figure S3を確認してみました。
No hemorrhageではちょうど1程度ですが、Haemorrhageでは(blood O2 sat>85%, <=85%とも)ややPLEXに引っ張られているように見えました。肺胞出血を伴うような重症例ではPLEXの効果はまだ完全には消えていないのかもしれません。同様の事はCreatinin≧5.6 mg/dlでも言えるかもしれないですね。Uptodateでは肺胞出血の全例ですべきとは言わないが、標準治療に抵抗する場合は考慮する、というスタンスでした。ごもっとも、と思いました。