EULAR recommendations: 2016 updateが出版されました。
最初にTable2を訳して、つぎにMethodを訳しています。
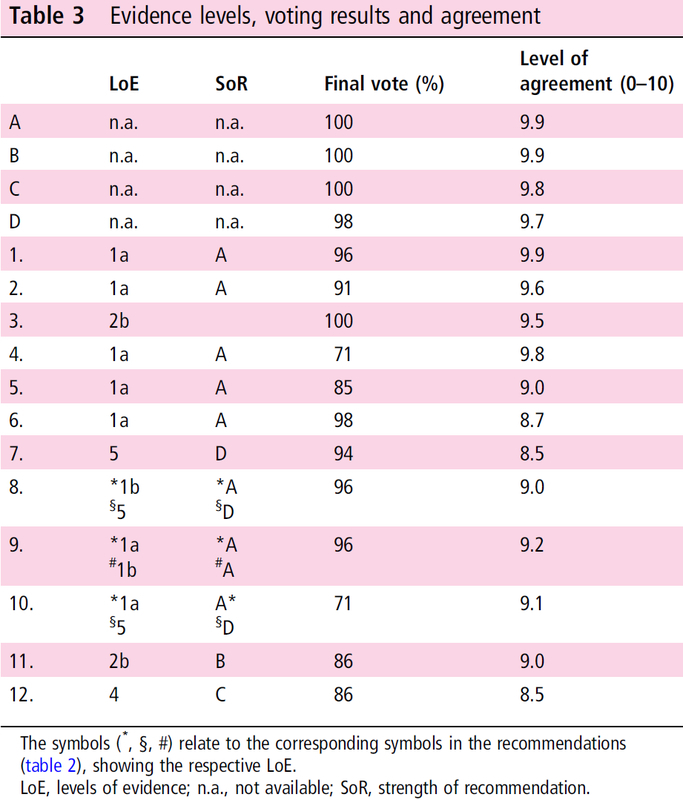
Table 2
The 2016 EULAR updated recommendations
2016年改訂EULARrecommendations
Overarching principles包括的指針
A. Treatment of patients with RA should aimat the best care and must be based on a shared decision between the patient andthe rheumatologist
RA患者の治療はベストな管理を目標とされるべきであり、患者とリウマトロジストとの共有された意志決定に基づくべきである。
B. Treatment decisions are based on diseaseactivity and other patient factors, such as progression of structural damage,comorbidities and safety issues
治療は疾患活動性、および構造的破壊の進行、合併症、安全性の問題といったその他の患者のファクターに基づいて決定されるべきである。
C. Rheumatologists are the specialists whoshould primarily care for patients with RA
リウマトロジストはRA患者のプライマリーケアを行うべき専門医である。
D. RA incurs high individual, medical andsocietal costs, all of which should be considered in its management by thetreating rheumatologist
RAは個人において、医療において、社会的にも高いコストを招き、これらは治療するリウマトロジストによる管理のもと考慮されるべきである。
Recommendations
1. Therapy with DMARDs should be started assoon as the diagnosis of RA is made
DMARDsによる治療はRAの診断がつき次第開始されるべきである。
2. Treatment should be aimed at reaching atarget of sustained remission or low disease activity in every patient
治療の目的は全ての患者において持続する寛解あるいは低疾患活動性を達成することであるべし。
3. Monitoring should be frequent in activedisease (every 1–3 months); if there is no improvement by at most 3 months afterthe start of treatment or the target has not been reached by 6 months, therapyshould be adjusted
活動性のあるRAではモニタリングは1-3ヶ月毎のように頻繁であるべきだ;そしてもし治療開始して長くても3ヶ月後までに改善がない場合、あるいは6ヶ月までにターゲットが達成されない場合、治療を変更すべきである。
4. MTX should be part of the firsttreatment strategy
MTXは最初の治療戦略の一部であるべきである。
5. In patients with a contraindication toMTX (or early intolerance), leflunomide or sulfasalazine should be consideredas part of the (first) treatment strategy
MTXの禁忌を有する患者(または早期の不耐の患者)においてはレフルノミドまたはスルファサラジンを最初の治療戦略の一部として考慮すべきである。
6. Short-term glucocorticoids should beconsidered when initiating or changing csDMARDs, in different dose regimens androutes of administration, but should be tapered as rapidly as clinicallyfeasible
短期間のグルココルチコイドは様々な投与量・投与方法においてcsDMARDsw開始・変更する際に考慮されるべきである。ただし、臨床的に実行可能である限りできるだけ早期に減量するべきである。
7. If the treatment target is not achievedwith the first csDMARD strategy, in the absence of poor prognostic factors,other csDMARDs should be considered
治療目標が最初のcsDMARDの戦略で達成されなければ、予後不良因子がない場合はその他のcsDMARDsを考慮すべきである。
8. If the treatment target is not achievedwith the first csDMARD strategy, when poor prognostic factors are present,addition of a bDMARD*1,2 or a tsDMARD*3 should be considered; current practicewould be to start a bDMARD§
9. bDMARDs*1,2 and tsDMARDs#3 should becombined with a csDMARD; in patients who cannot use csDMARDs as comedication,IL-6 pathway inhibitors and tsDMARDs may have some advantages compared withother bDMARDs
bDMARDsとtsDMARDsはcsDMARDsと併用するべきであるが、csDMARDsを補助的に用いることができない患者ではIL6経路阻害薬とtsDMARDsがその他のbDMARDと比べていくらかの利益があるかもしれない。
10. If a bDMARD* or tsDMARD§ has failed,treatment with another bDMARD or a tsDMARD should be considered; if oneTNF-inhibitor therapy has failed, patients may receive another TNF-inhibitor oran agent with another mode of action
bDMARDsとtsDMARDsが失敗に終われば、その他のbDMARDかtsDMARDを考慮すべきだ;もし一つのTNF阻害薬が失敗すれば、患者は別のTNF阻害薬を受けるか、作用機序の異なる薬剤を受けるかもしれない。
11. If a patient is in persistent remissionafter having tapered glucocorticoids, one can consider tapering bDMARDs,especially if this treatment is combined with a csDMARD
12. If a patient is in persistentremission, tapering the csDMARD could be considered
患者が持続的な寛解にある場合、csDMARDの減量を考慮してもよいかもしれない。
(footnote)
1. TNF阻害薬: adalimumab, certolizumabpegol, etanercept, golimumb, infliximab
boDMARDs or the respectiveEMA-approved/FDA-approved biosimilars.
2. Abatacept, rituximab (特殊な状況下では最初のbDMARDとして—詳細はtextをみること), あるいはtocilizumab or respectiveEMA-approved/FDA-approved biosimilars, as well as other IL-6 pathwayinhibitors, sarilumab and/or sirukumab, once approved.
3. Jak阻害薬(承認されている場所では).
boDMARDs, biological originator DMARDs;
bsDMARD, biosimilar DMARDs;
csDMARDs, conventional synthetic DMARDs;
DMARDs, disease-modifying antirheumaticdrugs;
EULAR, European League Against Rheumatism;
Jak, Janus kinase;
MTX, methotrexate;
RA, rheumatoid arthritis;
TNF, tumour necrosis factor;
tsDMARDs, targeted synthetic DMARDs.
(Table 1よりpoor prognostic factors)

METHODS
EULAR実行委員会の承認後、会議の議長(JSS)とmethodologist(RL)はこのRA管理のEULAR recommendationのアップデートの仕事をする運営委員会とTask Forceを招聘した。2010年のrecommendationとその2013年のアップデートはEULARオリジナルのrecommendation開発のための標準的操作手順にしたがって作成された。2016年アップデートは最近修正されたこれらの標準的方法にしたがった。これはAGREErecommendationsのupdated version、AGREE IIにも遵守するものである。
Steering Committee運営委員会
運営委員会はリウマトロジスト7名、患者代表1名と3人のフェローを含んだ。このグループは最初に3つのSLRsのためのresearch questionを作った。これらのSLRsのターゲットは、(i) 合成DMARDsの効果(単剤あるいは併用療法による効果。csDMARDsとの併用においても、bDMARDsとの併用においても)、およびステロイドの効果; (ii) 生物学的DMARDsの効果 (単剤またはcsDMARDsとの併用において)、そして(iii)biological DMARDsの安全性。この目的のため2013年に得られたoriginalのSLRsはstarting pointとしての役目を果し、2013-2016年の間に出版された論文に基づくアップデートを行った。治療ストラテジーにおいて新しい情報を現在のSLRsにおいて評価した。フォーマルな経済的な解析は行わなかったが、コストの問題はrecommendation作成の現在のstate of the art、抗リウマチ療法のコストの問題を扱ったEULAR独自の過去のSLR、biosimilarの出現とともに、プロセスを通して考慮された。
リウマチ学のフェロー3名(KC,JN,SR)はSLRsを行い、お互いの仕事をチェックした。SLRsは効果を調べるためのRCTと安全性のための登録データについて現存する出版データを利用し、最近のEULARand ACRの会議のabstractも評価した。Task Forceと方法論の詳細を記載した3つのSLRが別々に出版された。Summary of findings (SoF) tablesが作られ、Level of evidence (LoE)はEBMのためのOxfordセンターの基準に沿って決定された。
SLRsのSoFは実行委員会にプレゼンされた。実行委員会はこの情報に基づいて推奨のアップデートのための提案を考案した。ついでSLRのデータと実行委員会の提案がTask force全員にプレゼンされ、さらなるdiscussionと最終的なrecommendationのアップデートが作成された。
Task Force
Task Forceは実行委員会を含む50名からなる。Task Forceメンバーの中には3人の患者、2名の医療従事者と2人のEULAR young rheumatologists’ network、EMEUNETの2名の代表が含まれていた。リウマトロジストは全員RAの治療において経験豊富であり、ほとんどが臨床試験に頻繁に参加していた;さらに数人は彼らの国において患者レジストリーにおける経験、様々なアウトカムのリサーチにおける経験を持っていた。患者と医療獣医者は全員合意形成の活動における経験を有していた。リウマトロジストのほとんどはもちろん。私たちはTask Forceの仕事がリウマトロジストによって世界中のその他の地域のリウマトロジストにも認知されることを願っていたため、ヨーロッパの14ヶ国の広範囲の代表者だけではなく、アジアから2名、オーストラリアから1名、ラテン・アメリカから2名、北アメリカから2名に参加するように招待した。彼らの数人は彼らの地域の学会and/or国家の活動に積極的に参加していた。全てのTask Forceメンバーがプロセスの始まる前に彼らの可能性のあるCOIを宣言した。
Task Forceは2-3の主な考えに前もって同意をした。まず全てのrecommendationsは新しいエビデンスとともに協議される必要があった;新しいエビデンスがない領域では以前のエビデンスがフォローされた。二番目に過去のrecommendations(4つの包括的な指針と14のrecommendations)のいずれも2013年バージョンにおいてプレゼンされたのと同じように維持することも、補正されることも、順序を変えられることも、削除されることも可能とされた。三番目にヨーロッパでまだ承認されていないが世界中の他の地域で使用される薬剤、あるいは規制された評価は行われていないが臨床試験のエビデンスが分かっている薬剤もrecommendationの考慮に入れて良いこととした。臨床現場における理解の期待と全ての各の警告を考慮できるように。最終的に2013年の推奨が、新たなエビデンスで支持された、または新しい情報が不足した全ての推奨が過去に言葉に表現されたように含有されることに合意があった。特定のコンポーネントが不適切と考えられない限り。
SLRの結果のプレゼンと実行委員会の推奨の修正案の提案ののちTask Forceは4つのbreakoutのグループに分かれた。ひとつのグループはbDMARDs、二つ目のグループはcsDMARDs、三つ目のグループはtsDMARDs、そして4つめのグループはステロイドのグループであった;全てのグループは各のrecommendationについての草案の文章を全てのTaskForceに提案した。安全性の問題についてはこの各のbreakoutグループに向けられた。
Consensus finding合意
各のブレークアウトの代表は各の審議の結果を報告し、全てのTask Forceに対して個々のrecommendationの言語かについての提案をプレゼンした。その後、投票のプロセスが行われた。
包括的指針やrecommendationがさらなる修正なしの最終の文章としてアクセプトされるために、投票の75%の大多数が最初の投票では必要とされた。もしこれが達成されなければ各の文章を修正し、2回目の投票が行われた。2回目の投票では67%の賛成が必要とされた。もしこれでも上手くいかなかったらさらなる用語の修正が行われ、50%以上の賛成が得られるまで提案された。recommendationは最終的な投票として提示された。各の最後の投票の結果は投票メンバーの%で示された。ノートは会議録を記録し、各の項目に関連するコメントに提示された決断の理由を含んだ。様々な理由で全てのTask Forceメンバーが会議中ずっと部屋にいたわけではない。そのため投票数には少々の多様性があった。しかし、全てのポイントにおいて>90%のメンバーが投票に参加した。
対面会議においてTask Forceで同意された推奨はemailで同意レベル(the levels of agreement , LoA)による無記名投票を受けた。各の推奨は同意しないを0、完全な同意を10とした0-10のスケールの裁決を受けた。会議の数週間後のこのプロセスの間、ひとりがTaskForceから離脱した。理由は先の投票プロセスの間、csDMARDの併用療法が多数決で否定されたことが分かったため。この人は期間中会議に参加し投票を行った。全ての推奨に関する各々の投票は考慮に入れられたが、最終的にその人はauthorshipを拒否したため、この人の票はLoAに反映されたないものとした。
論文の草案は全てのTask Forceメンバーに送られ、コメントを求められた。それらのコメントを組み入れた後、EULAR executive committeeに提出されレビューと承認を求められた;この時点で再度Task Forceメンバーに送られた。最終的な意見はTask ForceメンバーとExecutive committeeから得られ、本雑誌の投稿規定に合わされた。それからEULAR executive committeeによって投稿され承認された。