MPAで治療中の70代男性。GCパルス→PEXIVAS (reduced)で開始したところ、1ヶ月でCMV感染症による急性肝炎を発症した。なぜ、このようなことになったのか・・・
pubmedで、cytomegalovirusとANCAで検索したところ、本邦よりCMV感染の危険因子を検討した多施設コホート研究が最近、報告されていた。
Risk Factors for Cytomegalovirus Reactivation during the Treatment of ANCA-Associated Vasculitis: A retrospective cohort study of the J-CANVAS study.
Kawamori K, et al.
https://pubmed.ncbi.nlm.nih.gov/39887020/
Materials and methods
Study design and settings
January 1st, 2017 to June 30, 2020に登録された、後ろ向き コホート、 the Japan Collaborative Registry of ANCA-associated vasculitis (J-CANVAS). 日本の24施設より登録された新規or再燃のAAV。
登録条件は≥20 years 、MPA and GPA の最初のエピソードで、CHCC 2012[1] とthe European Medicines Agency Algorithm [12] を満たすこと。
CMV感染の危険因子を明らかにするため最初の寛解導入療法を対象とし、再発患者は除外.
Risk factors
寛解導入時のpotential risk factors for CMV reactivationを集めた;治療開始時のlaboratory data, 疾患(MPA and GPA), ANCA型, DM/CKDのような併存疾患。疾患活動性と臓器障害を評価するため、the Birmingham Vasculitis Activity Score (BVAS)を抽出した: general, cutaneous, mucous membranes/eyes, ear, nose and throat, chest, cardiovascular, abdominal, renal, and nervous system [14=BVAS version 3]. 体重当たりの初期GC投与量、mPSL pulse, IS, PEも。
Outcomes
primary outcome はAAV治療開始後のCMV reactivation(臓器症状は問わない、48wまでのウイルス抗原陽性で定義)。CMV reactivation は1個のウイルス抗原陽性細胞で定義。The frequency of CMV antigen testing, whether or not the test was performed, and when the test was first performed were left to the discretion of each institution; its treatment was also left to the discretion of the attending physician. CMV抗原検査の頻度、検査の有無、初回検査の時期などは各施設の裁量に任され、その治療も主治医の裁量に任されていた。The HRP-C7 and C10/C11 methods のいずれも可とした。
Statistical analysis
Patient characteristics
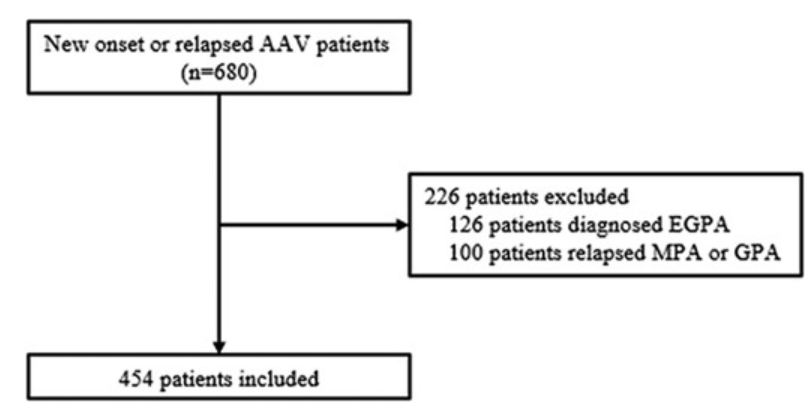
454例のうち65例はCMV検査をされていなかったが、no CMV reactivationとみなした。
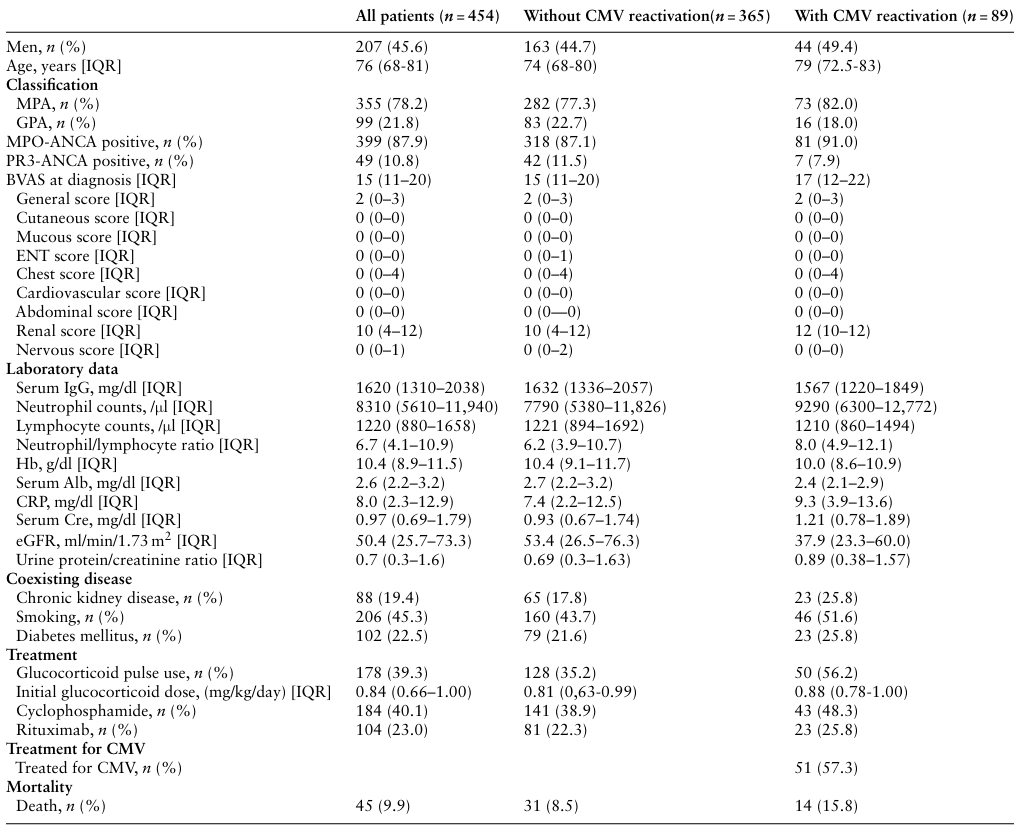
CMV reactivation
CMV再活性化は89例(19.6%)で観察された。 最初に測定されたCMV抗原の再活性化は、治療開始後27.5日(IQR、20~39.5日)であり、80%以上の患者が2ヵ月以内に再活性化を示した。
Risk factors of CMV reactivation
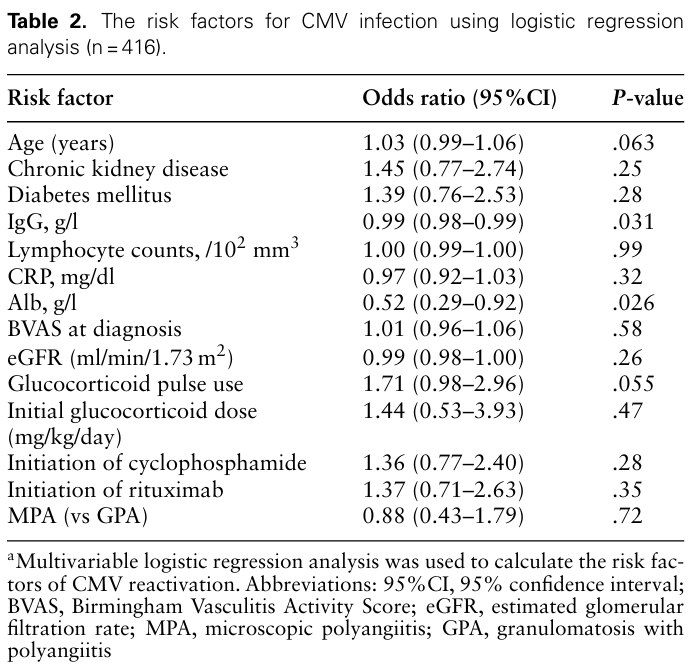
CMV再活性化患者は非再活性化患者より年齢が高く(79歳 vs 74歳、P < 0.001)、疾患活動性のBVASスコアが高く(17 vs 15、P = 0.004)、各臓器のBVAS腎スコアが高かった(12 vs 10、P < 0.001;Table 1)。 初回検査の結果、好中球数が多い患者(9290 vs 7790/μl、P = 0.02)、好中球/リンパ球数の比が高い患者(8.0 vs 6.2、P = .008)、低アルブミン(2.4 vs 2.7g/dl、P = .002)、高クレアチニン(1.21 vs 0.93mg/dl、P = .005)、低eGFR(37.9 vs 53.4ml/min/1.73m2、P = .005)では、CMV再活性化が多かった。GCパルス療法は、CMV再活性化患者でより頻繁に行われた(56.2% vs 35.3%、P = 0.004)。 Table 2はLogistic regression analysisの結果であり、低アルブミン血症[OR 0.52、95%CI:0.29-0.93]、血清IgG低値(OR:0.99、95%CI:0.99-0.99)がCMV再活性化の危険因子であることが明らかになった。 CMV再活性化が明確に測定された患者を対象とした感度分析でも同様の結果が示され、診断時年齢が高いこと(OR 1.03、95%CI:1.00-1.06)、低アルブミン血症(OR:0.51、95%CI:0.28-0.91)、血清IgGが低いこと(OR:0.99、95%CI:0.99-0.99)がCMV再活性化のリスク因子であることが示唆された。
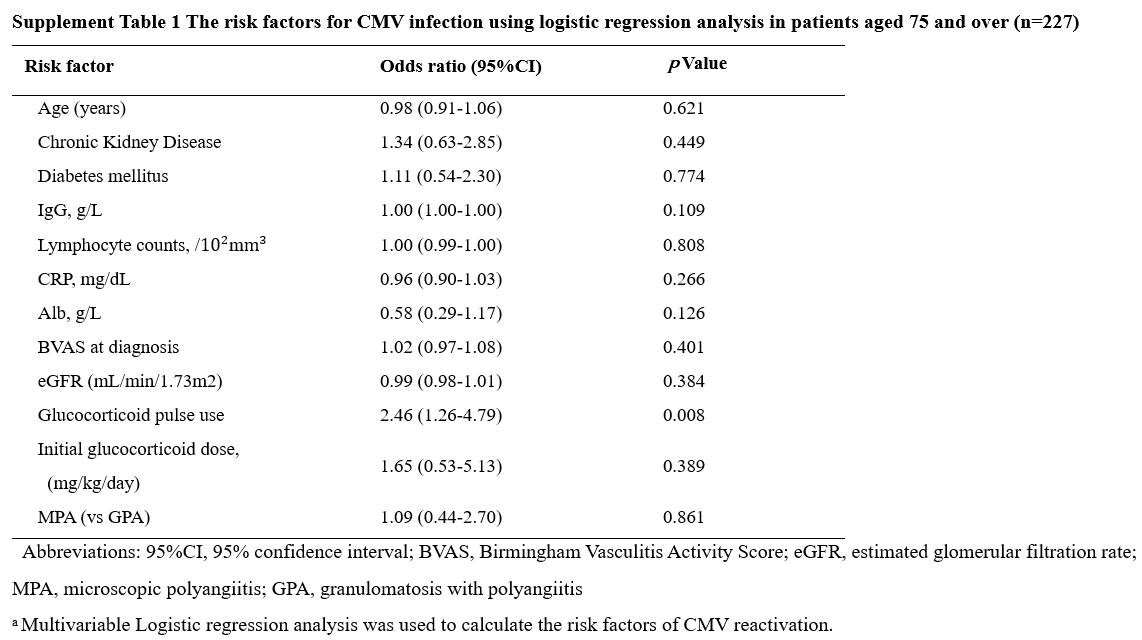
さらに、75歳以上の高齢者のみからなる群(227人)を対象としたロジスティック回帰分析では、CMV感染の有無を従属変数とした場合、ステロイドパルス療法の実施はCMV再活性化のリスク上昇と関連していた (OR: 2.46, 95% CI: 1.26–4.79) (Supplement Table S1)。
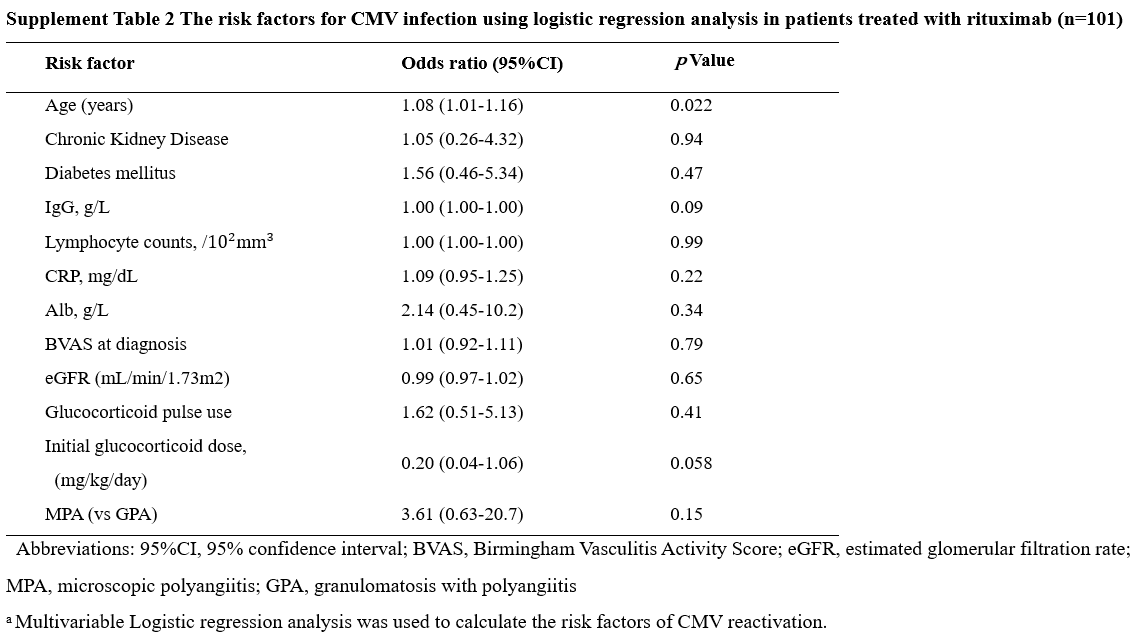
同様に、リツキシマブ使用者のみからなる群(101人)のロジスティック回帰分析においても、年齢はCMV再活性化と有意かつ正の相関を示した (OR: 1.08, 95% CI: 1.01–1.16) (Supplement Table S2).
<まとめ>
多変量解析で、全体集団ではIgG1g/L上がるごとにOR 0.99(p=0.031)、Alb1g/LあがるごとにOR 0.52は有意(p=0.026)。年齢1歳↑は1.03(p=0.063)、Pulse有はOR 1.7 (p=0.055)と傾向あり
2つのサブグループをしてくれていて、
75歳以上ではPulse有のOR 2.46 (p=0.008)と唯一有意
RTX使用の場合、年齢1歳↑はOR 1.08 (p=0.022)、初期GC1mg/kg/day↑ごとにOR 0.20 (p=0.058)と傾向あり